螺旋藻穿上磁性外衣,由磁场引路,能准确到达肿瘤组织,并通过光合作用提供氧气。浙江大学科学家日前研制出的这款有机和无机相结合的微纳机器人,提供了生物杂化材料体内应用的新前景。相关论文刊发在材料领域著名期刊《先进功能材料》(Advanced Functional Materials),并被遴选为当期封面。
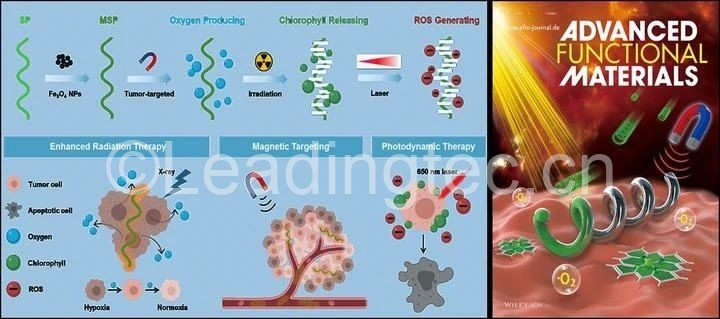
微纳机器人是一种尺度介于微纳米级别,可以对微纳空间进行精细操作的机器人。浙大医学院附属第二医院/转化医学研究院周民研究员团队研制的这款微纳机器人以螺旋藻作为活体支架,“穿上”磁性涂层外衣,靶向输送至肿瘤组织,成功改善肿瘤乏氧微环境并有效实现磁共振/荧光/光声三模态医学影像导航下的肿瘤诊断与治疗。肿瘤细胞在快速增殖中消耗了大量的氧气,导致肿瘤组织内部存在缺氧微环境,这成为众多肿瘤治疗方法出现耐受现象的重要原因之一。据了解,一般临床肿瘤治疗采用的放疗和光动力治疗中,患者通过高压氧仓吸氧来解决肿瘤内部氧气不足的问题。但这种方法往往收效甚微,并不能达到靶向供氧到肿瘤部位,难以提高肿瘤治疗效果。螺旋藻是一种生活中常见的微藻,作为水生植物能够通过光合作用产生氧气。周民团队将超顺磁性的四氧化三铁纳米颗粒通过浸涂工艺,均匀涂层至微藻表面。磁性工程化的微藻在外部磁场控制下,就能定向运动至肿瘤。“研究的创新性在于无机和有机的微纳体,选择性把药物输送到肿瘤缺氧部位。”周民介绍,他们所研制的微纳机器人是一种光合生物杂交体系统,这个系统既保持了微藻高效的产氧活性,还兼有四氧化三铁纳米颗粒的定向磁驱能力。在具体治疗中,通过体外交变磁场将微纳机器人靶向运送并积累至肿瘤,通过体外光照,由光合作用原位产生氧气来减轻肿瘤内部乏氧程度,从而提高放射疗法的效率。“在小鼠的原位乳腺癌模型中,经增强的联合治疗展现了明显的肿瘤生长抑制作用。”
光合生物杂交微纳泳体系统不仅对于放疗具有积极作用,在经过射线处理后释放的叶绿素能作为光敏剂,进而产生具有细胞毒性的活性氧来杀死肿瘤细胞,实现协同光动力治疗。“正常的光动力治疗需要氧气和活性氧才能顺利开展,目前的微纳机器人能够很好地解决这两个需求。”
此外,微藻中含有的大量叶绿素,也具有的天然荧光和光声成像功能,可以无创性地监测肿瘤治疗情况和肿瘤微环境变化。“药物遇到荧光,就能够表达出来。叶绿素此时就像一面镜子。”
这项研究持续了三年,周民说最早关注到微藻是源于一次海洋学院会议,和藻类研究的朋友聊天时受到的启发。面对未来的应用前景,周民说:“该微纳泳体本质作为天然生物能够在体内得到有效降解,为生物杂化材料应用在靶向递送和体内生物医学中提供了转化前景。”